Normaal bestaan de covalente bindingen in koolstofmoleculen uit twee elektronen. Nu schijnen er ook stabiele bindingen te bestaan tussen koolstofatomen die maar uit een elektron bestaan, zagen Japanse onderzoekers.
Covalente bindingen, waarbij twee atomen aan elkaar gebonden zijn door een elektronenpaar te delen, vormen de basis voor de meeste organische verbindingen. In 1931 dacht Nobelprijswinnaar Linus Pauling al dat covalente bindingen met slechts één, ongepaard elektron ook zouden kunnen bestaan, maar deze enkelvoudige elektronbindingen zouden waarschijnlijk veel zwakker zijn dan een standaard covalente binding met een elektronenpaar, dacht Pauling.
Sindsdien zijn enkelvoudige elektronbindingen waargenomen, maar nooit in koolstof of waterstof. Nu hebben onderzoekers van de Universiteit van Hokkaido dan toch een verbinding geïsoleerd waarin één enkel elektron wordt gedeeld door twee koolstofatomen in een opmerkelijk stabiele covalente binding, bekend als een sigmabinding.
“Het verduidelijken van de aard van enkelvoudige elektron sigmabindingen tussen twee koolstofatomen is essentieel om een beter begrip te krijgen van chemische bindingstheorieën en zou meer inzicht bieden in chemische reacties”, legt scheikundige Yusuke Ishigaki uit.
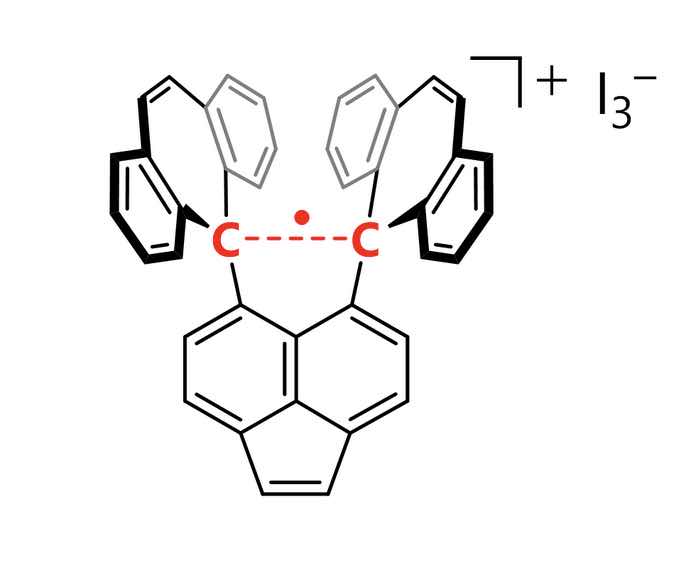
De enkelvoudige elektronbinding werd gevormd door een derivaat van hexafenylethaan, dat een extreem uitgerekte covalente binding met gepaarde elektronen tussen twee koolstofatomen bevat, te oxideren in aanwezigheid van jodium. De reactie produceerde donkerpaarse kristallen van een jodiumzout.
De onderzoekers gebruikten röntgendiffractieanalyse om de kristallen te bestuderen en ontdekten dat de koolstofatomen erin extreem dicht bij elkaar lagen, wat suggereert dat er covalente eenelektronbindingen tussen koolstofatomen aanwezig zijn. Ze konden dit vervolgens bevestigen met behulp van de Raman-spectroscopie.
Shimajiri: “Deze resultaten vormen dus het eerste experimentele bewijs voor een covalente eenelektronkoolstof-koolstofbinding, waarvan verwacht kan worden dat het de weg vrijmaakt voor verdere ontwikkelingen van de chemie van dit nauwelijks onderzochte type binding.” Ben benieuwd.
Bron: Science Daily